Notions de base :
Métabolisme, catabolisme et anabolisme
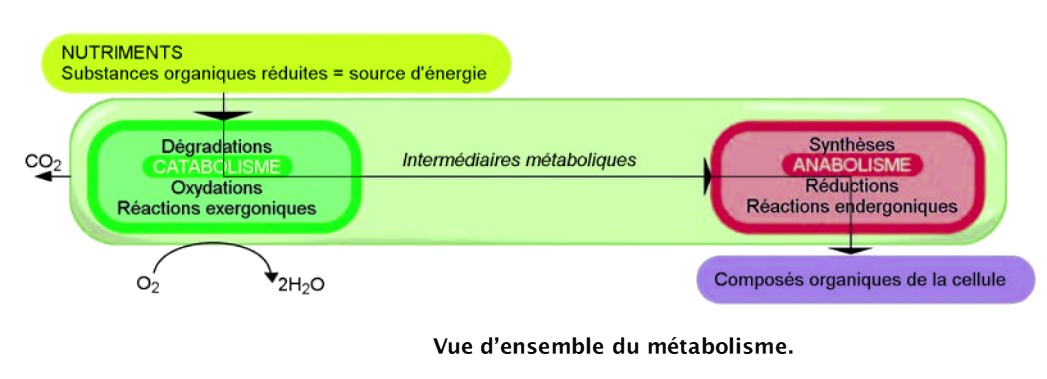
Le métabolisme comprend toutes les réactions biochimiques qui participent à la survie, à la multiplication et à la croissance des cellules qui constituent un organisme.
On distingue :
- le catabolisme (dégradation, production d’énergie)
- l’anabolisme (synthèse, utilisation ou stockage d’énergie).
L’ensemble de ces réactions est dépendant des échanges de matière et d’énergie entre environnement et organisme.
Bioénergétique
Les organismes vivants sont donc des systèmes ouverts sur le plan thermodynamique. L’étude des transferts d’énergie dans et entre les organismes vivants s’appelle la bioénergétique.
Hétérotrophes
Les êtres humains sont hétérotrophes Ils produisent de l’énergie à partir de molécules organiques synthétisées par des organismes autotrophes (végétaux) à partir de l’énergie solaire et de CO2.
Équilibre énergétique
Le principe d’équilibre énergétique consiste à égaliser les apports et les pertes énergétiques.
- Pour l’apport d’énergie, l’espèce humaine dépend exclusivement des sources nutritionnelles ‘l’alimentation’ et de l’utilisation des réserves corporelles.
- Les pertes d’énergie sont quant à elles de plusieurs types : production de chaleur et de travail (mécanique, enzymatique…).
Énergie libre
La première loi de la thermodynamique nous apprend que la quantité d’énergie interne ΔE d’un organisme évolue en fonction de la quantité de chaleur ΔQ et de la quantité de travail ΔW échangées avec son environnement: ΔE = ΔQ +ΔW, avec ΔE, ΔQ et ΔW exprimées en joules.
Joules et calories
L’unité internationale pour quantifier une quantité d’énergie est le joule (J) qui équivaut à 1 watt·seconde ou à 0,24 calorie, utilisée en nutrition et en diététique.
« … Quand une molécule organique « brûle », elle libère de l’énergie sous forme de chaleur. La quantité d’énergie totale contenue dans le composé est appelée enthalpie (H). Une partie seule¬ment de cette énergie, appelée énergie libre (G), peut être utilisée pour fournir un travail. Dans des conditions standard (25 °C, pH 7), G est appelée Go.
Une réaction biochimique A → B est dite exergonique quand elle produit de l’énergie. La variation d’énergie libre de cette réaction ΔGo ou (GB-GA) est négative. À l’inverse, elle est endergonique si ΔGo est positif… »
Couplage énergétique
L’énergie produite lors des réactions de catabolisme ne peut être utilisée directement par les systèmes biologiques. Des systèmes de couplage sont nécessaires afin de transformer l’énergie contenue dans les nutriments en énergie utilisable. Ces systèmes de couplage font intervenir des nucléotides possédant deux ou trois groupements phosphate. La particularité de ces molécules est que la liaison phosphate est riche en énergie.
Ainsi, la dégradation de nutriments tels que des glucides simples ou des acides gras produit de l’énergie (réaction exergonique) qui est utilisée pour transformer une molécule d’adénosine diphosphate (ADP) en adénosine triphosphate (ATP).
Cette molécule énergétique d’ATP constitue une sorte de monnaie d’échange utilisable par les multiples voies du métabolisme cellulaire.
Lors d’une réaction d’hydrolyse, l’ATP perd un ion phosphate et libère de l’énergie, qui est utilisée dans des réactions endergoniques telles que la synthèse de composés biochimiques (protéines, polyholosides…), pour fournir un travail mécanique (contraction musculaire…) ou pour des transports actifs (pompe Na+/K+…).
- ATP + H2O → ADP + H3PO4 (ΔGo = − 30,5 kJ)
- ADP + H2O → AMP + H3PO4 (ΔGo = − 30,5 kJ)
D’autres molécules, comme la créatine phosphate (créatine-P), possèdent également des liaisons riches en énergie. L’hydrolyse du groupement phosphate permet de synthétiser l’ATP à partir d’ADP selon la réaction:
-
Créatine-P + ADP ~ ~ Créatine + ATP.
![]()
Le métabolisme énergétique cellulaire
Seules certaines cellules peuvent stocker l’énergie, toutes sont capables de métaboliser les nutriments pour produire de l’ATP.
Catabolisme et synthèse d’ATP
Le glucose, les acides aminés ou les acides gras peuvent être utilisés par le métabolisme pour la synthèse d’ATP.
Elle peut s’effectuer en présence de dioxygène (aérobie) ou en son absence (anaérobie), avec un moins bon rendement dans cette dernière condition.
Au cours des réactions de synthèse d’ATP, des molécules NADH et le FADH2 sont également produites ; elles permettent le transport d’électrons à haute énergie.
Catabolisme du glucose
Le glucose, après son entrée dans la cellule, subit dans le cytosol une succession de réactions biochimiques qui fournit deux molécules de pyruvate, deux ATP et deux NADH. Cette transformation du glucose en pyruvate s’appelle la glycolyse.
- En conditions anaérobie, le pyruvate est transformé en lactate et les NADH sont oxydés en NAD+.
- En condition aérobie, le pyruvate est transporté vers la matrice mitochondriale où il est converti en acétylcoenzyme A (acétylCoA). L’ acétylCoA réagit avec l’acide oxaloacétique pour former de l’acide citrique.
- Le cycle de l’acide citrique (ou cycle de Krebs) transforme grâce à une succession de réactions biochimiques, une molécule de citrate en un oxaloacétate et produit de l’ATP, du NADH, du FADH2 et du CO2.

Le métabolisme cellulaire du glucose avec la glycolyse cytosolique, le cycle de Krebs et la chaîne respiratoire mitochondriale. Des molécules d’acétylCoA sont synthétisées à partir de la ß-oxydation des acides gras (hélice de Lynen) et d’acides aminés (exemple : l’alanine).
Les transporteurs d’électrons NADH et FADH2 transfèrent ensuite leurs électrons de haute énergie à des transporteurs d’électrons de la membrane interne mitochondriale dans une chaîne de réaction appelée phosphorylation oxydative ou chaîne respiratoire.
L’énergie des électrons permet de transporter des protons H+ de la matrice vers l’espace inter-membranaire mitochondrial. Le gradient de H+ permet ensuite d’alimenter l’ ATP synthétase, une enzyme synthétisant l’ATP.
Le bilan global théorique est de 38 molécules d’ATP synthétisées par molécule de glucose en condition aérobie, dont 2 par la glycolyse, 2 par le cycle de Krebs et 34 par la chaîne respiratoire.
Catabolisme des triglycérides
La dégradation des triglycérides débute par la libération des acides gras du glycérol. Le glycérol obtenu peut intégrer la glycolyse à mi-chemin.
Les acides gras sont pour leur part transportés vers la matrice mitochondriale où ils subissent un processus de Beta-oxydation leur permettant de produire de l’acétylCoA et d’intégrer ensuite le cycle de Krebs.
Le bilan de la beta-oxydation dépend du nombre d’atomes de carbone et du nombre de double liaison des acides gras.
Les acides gras permettant la production d’un grand nombre d’acétylCoA, ils sont plus énergétiques que le glucose.
L’acide oléique qui possède 18 atomes de carbone permet ainsi la synthèse de 144 molécules d’ATP, soit environ 8 molécules d’ATP par atome de carbone ; le glucose, une molécule à 6 atomes de carbone fournit 38 molécules d’ATP, soit environ 6 ATP par carbone.
Catabolisme des acides aminés
Les acides aminés peuvent également participer à la synthèse d’ATP. Ils peuvent générer, lors de réactions de désamination, des molécules telles que le pyruvate, qui peuvent ensuite intégrer la glycolyse et le cycle de Krebs. Cette réaction de désamination s’accompagne de production d’ammoniaque NH3, transformé en ions ammonium NH4 +. Ce produit toxique est transformé en urée CO(NH2)2 par le foie et éliminé dans les urines.
![]()
Stockage et utilisation des réserves
Le glucose
Le glucose peut être mis en réserve dans l’organisme sous forme d’un polymère glucidique ramifié, le glycogène. Ce processus essentiellement assuré par le muscle strié et le foie est appelé glycogénogenèse.
Elle implique différentes enzymes qui permettent la transformation du glucose (phosphorylation, isomérisation et ajout d’UDP), l’élongation de la chaîne de glycogène et sa ramification. Les réserves énergétiques stockées dans le glycogène peuvent être mobilisées par un processus de dégradation permettant la libération du glucose. Ce processus catabolique de glycogénolyse, opposé à la glycogénogenèse, possède son propre équipement enzymatique. Le glucose peut d’autre part être produit dans le foie et le rein à partir de molécules non glucidiques (lactate, acides aminés, glycérol) au cours de la néoglucogenèse (aussi appelé gluconéogenèse).
Les lipides
Les acides gras circulants peuvent être stockés dans les cellules et notamment les adipocytes sous forme de triglycérides au cours du processus de lipogenèse. La dégradation des triglycérides en acides gras s’appelle la lipolyse et permet d’alimenter le métabolisme cellulaire, aboutissant à la synthèse d’ATP, via la beta-oxydation des acides gras.
![]()
Le métabolisme : -vue d’ensemble
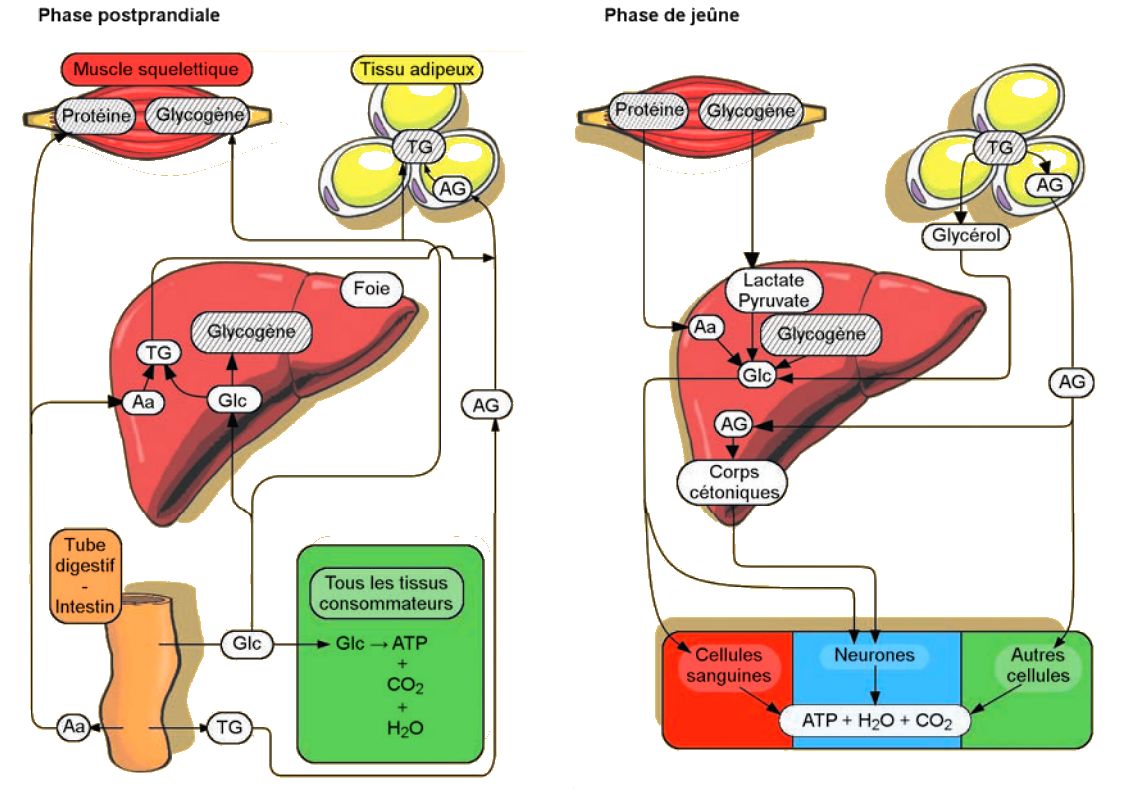
À l’échelle de l’organisme, le métabolisme dépend de différents organes (foie, muscles squelettiques, tissu adipeux) spécialisés dans différents métabolismes (glucides, lipides, protides), de systèmes régulateurs (hormonaux et nerveux) et de l’apport ou non en aliments, définissant des phases métaboliques postprandiale (littéralement à la suite du repas) et de jeûne.
État postprandial
À la suite d’un repas s’opèrent les mécanismes de digestion participant à fournir des nutriments à l’organisme. L’abondance de nutriments pendant la période postprandiale conduit à leur mise en réserve afin de palier les périodes de carences ultérieures.
Au cours de cette phase,
- le foie et les muscles striés mettent en réserve, par glycogénogenèse, le glucose circulant sous forme de glycogène.
- Les lipides circulants pour leur part sont stockés au niveau des adipocytes, essentiellement sous forme de triglycérides.
Les modifications métaboliques intervenant pendant cette phase sont en grande partie dues à une augmentation de la sécrétion d’insuline, seule hormone hypoglycémiante. Les acides aminés sont intégrés dans de nouvelles protéines (dont des protéines musculaires).
Au niveau du foie, une partie des molécules de glucose est transformée en acétylCoA. Il en est de même pour les acides aminés qui génèrent des acides alpha-cétoniques puis des molécules d’ acétylCoA. Ces dernières peuvent participer à la synthèse lipidique dans les cellules adipeuses.
Le stockage énergétique est limité quantitativement à environ 400 g de glycogène (environ 100 g dans le foie et 300 g dans le muscle) ou plus chez des sportifs (1 kg), soit 1 000 à 2000 kcal, ce qui représente une réserve énergétique de 24 h. Les triglycérides étant non hydratés (contrairement au glycogène hépatique ou musculaire), et beaucoup plus importants en quantité (10 à 15 kg chez des individus maigres), ils constituent une réserve énergétique considérable (environ 100 000 kcal, soit un à deux mois). Le rendement calorique est de 9,2 kcal·g−1 pour les triglycé¬rides contre 1,5 kcal·g−1 pour le glycogène de réserve.
Leur rôle énergétique n’étant pas leur fonction première, les protéines de structure de l’ organisme ne constituent pas à proprement parler des réserves mais peuvent cependant être recrutées lors de jeûnes prolongés.
État de jeûne
Le jeûne se définit comme une période de carence en apport nutritionnel une fois l’absorption des nutriments achevée, c’est-à-dire 4 à 5 h après un repas. Au cours du jeûne, l’organisme adapte son métabolisme à une diminution de l’apport nutritionnel de manière à permettre un apport énergétique aux cellules.
Certaines cellules dites « glucodépendantes » ne peuvent utiliser que le glucose comme substrat énergétique pour fabriquer de l’ATP. C’est le cas des hématies et des neurones (ces derniers pouvant également utiliser les corps cétoniques). Les autres cellules de l’organisme peuvent puiser dans les autres nutriments (et notamment les acides gras) afin de produire de l’ATP.
Trois phases différentes du jeûne sont distinguées:
Une phase glucidique immédiatement après la phase d’absorption. Au cours de cette phase, la glycogénolyse hépatique a lieu, ce qui permet aux cellules hépatiques de sécréter du glu¬cose et de maintenir la glycémie à un niveau physiologique. La glycogénolyse musculaire est incomplète et aboutit à la formation de glucose-6-phosphate, qui peut alimenter la glycolyse musculaire mais ne peut pas être transformé en glucose dans ces cellules. Concomitamment, la néoglucogenèse, stimulée grâce à la synthèse et l’activation d’enzymes, permet de synthétiser du glucose à partir de composés non glucidiques, notamment le glycérol provenant de la lipolyse, des acides aminés glucoformateurs (comme l’alanine ou la glutamine) et du lactate. Au cours de cette phase, la lipolyse est stimulée et permet de générer des acides gras à partir
des triglycérides des tissus adipeux.
Une phase de protéolyse intervient ensuite. Elle permet d’alimenter la néoglucogenèse et de fournir le glucose nécessaire aux cellules glucodépendantes. Cette phase commence rapidement (24 h) après que les stocks de glycogène ont été utilisés.
Une phase cétonique survient ultérieurement. Cette phase de cétogenèse permet d’épargner les réserves protéiques de l’organisme et entraîne la production de corps cétoniques à partir d’acides gras, utilisables par les neurones pour produire de l’ATP. Les modifications métaboliques intervenant pendant cette phase sont en grande partie dues à une diminution de la sécrétion d’insuline et à une augmentation de la sécrétion d’hormones hyperglycémiantes comme le glucagon, l’adrénaline et le cortisol.
Vue d’ensemble du métabolisme.
Les réserves sont indiquées en hachuré. TG = triglycéride, Glc = glucose, Aa = acides aminés, AG = acide gras.